Способы защиты от коррозии
Коррозия — это самопроизвольное разрушение металлов в результате химического или физико-химического взаимодействия с окружающей средой. В общем случае это разрушение любого материала, будь то металл или керамика, дерево или полимер.
Более всего подвержены коррозии чистые металлы. Сплавы, пластики и прочие материалы в этом отношении характеризуются термином «старение». Вместо термина «коррозия» также часто применяют термин «ржавление».
Виды коррозии
Коррозионный процесс портит жизнь людям многие века, поэтому он изучен достаточно широко. Существуют различные классификации коррозии в зависимости от типа окружающей среды, от условия использования коррозирующих материалов (находятся ли они под напряжением, если контактируют с другой средой, то постоянно или переменно и пр.) и от множества других факторов.
Электрохимическая коррозия
Коррозировать могут два различных металла, соединенных между собой, если на их стык попадет, например, конденсат из воздуха. У разных металлов различные окислительно-восстановительные потенциалы и на стыке металлов образуется фактически гальванический элемент. При этом металл с более низким потенциалом начинает растворяться, в данном случае, коррозировать. Это проявляется на сварочных швах, вокруг заклепок и болтов.
У разных металлов различные окислительно-восстановительные потенциалы и на стыке металлов образуется фактически гальванический элемент. При этом металл с более низким потенциалом начинает растворяться, в данном случае, коррозировать. Это проявляется на сварочных швах, вокруг заклепок и болтов.
Для защиты от такого вида коррозии применяют, например, оцинковку. В паре металл-цинк коррозировать должен цинк, но при коррозии у цинка образуется оксидная пленка, которая сильно замедляет процесс коррозии.
Химическая коррозия
Если поверхность металла соприкасается с коррозионно-активной средой, и при этом нет электрохимических процессов, то имеет место т.н. химическая коррозия. Например, образование окалины при взаимодействии металлов с кислородом при высоких температурах.
Борьба с коррозией
Несмотря на то, что сгнивающие на дне моря корабли с сундуками не так уж и плохи для экологии, коррозия металлов ежегодно приносит огромные убытки людям. Поэтому неудивительно, что уже давно существуют различные методы защиты от коррозии металлов.
Поэтому неудивительно, что уже давно существуют различные методы защиты от коррозии металлов.
Различают три вида защиты от коррозии:
Конструкционный метод включает в себя использование сплавов металлов, резиновых прокладок и др.
Активные методы борьбы с коррозией направлены на изменение структуры двойного электрического слоя. Применяется наложение постоянного электрического поля с помощью источника постоянного тока, напряжение выбирается с целью повышения электродного потенциала защищаемого металла. Другой метод — использование жертвенного анода, более активного материала, который будет разрушаться, предохраняя защищаемое изделие.
Пассивная борьба с коррозией – это применение эмалей, лаков, оцинковки и т.п. Покрытие металлов эмалями и лаками направлено на изоляцию металлов от окружающей среды: воздуха, воды, кислот и пр. Оцинковка (как и другие виды напыления) кроме физической изоляции от внешней среды, даже в случае повреждения ее слоя, не даст развиваться коррозии металла, т. к. цинк коррозирует охотнее железа (см. «электрохимическая коррозия» выше по тексту).
к. цинк коррозирует охотнее железа (см. «электрохимическая коррозия» выше по тексту).
Наносить защитные покрытия на металл можно различными способами. Оцинковку можно проводить в горячем цеху, «на холодную», газотермическим напылением. Окраску эмалями можно проводить распылением, валиком или кистью.
Большое внимание надо уделять подготовке поверхности к нанесению защитного покрытия. От того, насколько качественно будет очищена поверхность металла, во многом зависит успех всего комплекса мер по защите от коррозии.
Почвенная коррозия и защита от нее
Энциклопедия технологий
Проблема
Трубопровод, погруженный во влажный грунт, оказывается в агрессивной среде, которая способствует развитию коррозии. Прежде всего это связано с наличием воды, кислорода и различных веществ, растворяемых водой, что делает грунт средой, в которой проходят активные электрохимические реакции.
В отличие от атмосферной коррозии, почвенная коррозия характеризуется крайней неоднородностью — слабо корродирующие участки могут соседствовать с участками, где коррозия идет крайне активно. Это связано с влажностью грунта, его пористостью, воздухопроницаемостью и наличию в нем тех или иных веществ.
Это связано с влажностью грунта, его пористостью, воздухопроницаемостью и наличию в нем тех или иных веществ.
Решения
Наиболее радикальный и вместе с тем наиболее дорогой способ избавления от коррозии — это использование труб из нержавеющих сплавов или иных некорродирующих материалов. Однако такие сплавы дороги и применяются в ограниченном объеме. Можно также изменить окружающую среду трубопровода, например вместо погружения в грунт поместить его в особый бетонный короб или установить короб над ним. Старейшим и наиболее распространенным способом является нанесение на трубопровод гидроизолирующего покрытия.
Для этих целей применяют всевозможные мастики, которыми покрывают очищенные от загрязнений трубы, а затем укутывают их специальными пленками. Трубы могут гидроизолироваться как на месте их укладки, так и на заводе, что предпочтительнее. В заводских условиях есть возможность покрыть трубы специальными эмалями или пластиком, что обеспечит защиту металла на долгие годы. В ряде случаев, например при укладке трубопроводов по дну акваторий, трубы покрываются бетонной рубашкой. В полевых условиях будет необходимо заизолировать только зону сварного стыка.
В ряде случаев, например при укладке трубопроводов по дну акваторий, трубы покрываются бетонной рубашкой. В полевых условиях будет необходимо заизолировать только зону сварного стыка.
Еще один способ борьбы с коррозией трубопроводов — это электрохимическая защита. Она решает комплекс задач не только по борьбе с почвенной коррозией, но и с коррозией, вызванной блуждающими токами.
Так называемая «протекторная» защита обеспечивается установкой вместе с трубопроводом в той же среде болванок из металла, обладающего более электроотрицательными свойствами, чем железо, например из магния. В результате взаимодействия в электропроводящей среде разрушаться начнет именно он, а коррозия на поверхности стальных труб значительно замедлится. Более электроотрицательный металл называется «протектором», и этот метод широко применяется для защиты корпуса морских судов и конструкций.
Более интенсивным методом защиты трубопровода является принудительная катодная поляризация с применением внешних источников постоянного тока. Защищаемый трубопровод подключается в качестве катода к так называемой «станции катодной защиты». В свою очередь в грунт погружаются анодные элементы, которые и будут подвергаться анодному растворению. Этот метод отличается высокой эффективностью и может применяться как постоянно, так и периодически.
Защищаемый трубопровод подключается в качестве катода к так называемой «станции катодной защиты». В свою очередь в грунт погружаются анодные элементы, которые и будут подвергаться анодному растворению. Этот метод отличается высокой эффективностью и может применяться как постоянно, так и периодически.
В свою очередь, трубопроводы могут сами оказаться в зонах, где распространены так называемые блуждающие токи, образующиеся в результате утечек от различных источников — в частности электропроводящих рельсов электротранспорта. Для противодействия этому процессу, который приводит к крайне интенсивной коррозии трубопроводов, весьма распространенному в индустриальных зонах, применяется электродренажная защита, которая призвана предупредить возникновение блуждающих токов, и защитить сам трубопровод от их воздействий.
Коррозия и защита от коррозии объектов добычи, подготовки, транспорта и хранения нефти и газа
Программа имеет своей целью качественное изменение следующих профессиональных компетенций слушателей, необходимых для трудовой деятельности в рамках имеющейся квалификации:
- способность участвовать в реконструкции нефтегазопромыслового оборудования, систем и других объектов трубопроводного транспорта нефти и газа, применяя методы защиты от коррозии, с переводом их на новый технический уровень;
- способность проводить коррозионные исследования и электрометрические изыскания и рассчитывать параметры защиты от коррозии нефтегазопромыслового оборудования и трубопроводов;
- способность анализировать новые направления в разработке средств защиты от коррозии, использовать технологические приемы изменения состава и физико-химических свойств технологических сред с целью снижения коррозионной агрессивности;
- способность участвовать в совершенствовании существующих систем защиты от коррозии с учетом требований отраслевых нормативных документов;
- способность осуществлять эксплуатацию оборудования защиты от коррозии на объектах нефтегазопромыслового оборудования и трубопроводного транспорта нефти.

В результате освоения программы слушатель должен приобрести следующие знания и умения, необходимые для качественного изменения указанных компетенций:
слушатель должен знать:
- основы учения об электричестве, теории коррозии и применения защитных покрытий;
- основные виды коррозионных разрушений и причины их образования;
- основные методы электрохимической защиты и измерений;
- основные термины и определения в области коррозии металлов и сплавов;
- контроль качества защитных покрытий;
- требования к защитным покрытиям и их влияние на катодную защиту;
- особенности электрохимической защиты подземных и подводных металлических конструкций;
- методики измерений на подземных и подводных металлических конструкциях;
- методы анализа и оценки эффективности систем электрохимической защиты;
- методы защита от коррозии блуждающим током от систем постоянного тока;
- основные принципы защиты от коррозии внутренних поверхностей оборудования с применением ингибиторов коррозии;
- виды и физико-химические свойства ингибиторов коррозии;
слушатель должен уметь:
- выполнять контроль, проверку и испытания во время монтажа, технического обслуживания элементов системы электрохимической защиты;
- выбирать способы проведения измерений и испытаний в системах электрохимической защиты;
- выполнять работы по монтажу, плановому техническому обслуживанию систем электрохимической защиты;
- определять мероприятия по повышению эффективности электрохимической защиты;
- выполнять проектные работы по антикоррозионной защите;
- рационально выбирать коррозионностойкие материалы и защитные покрытия;
- рассчитывать систему защиты от коррозии;
- оценивать техническое состояние оборудования дозирования ингибитора коррозии.

Программа разработана на основе профессиональных стандартов:
- «Специалист по электрохимической защите от коррозии линейных сооружений и объектов», утвержденного приказом Минтруда России от 8 сентября 2014 г. №614н.
- «Специалист по защите от коррозии внутренних поверхностей оборудования нефтегазового комплекса», утвержденного приказом Минтруда России от 28 декабря 2015 г. №1166н.
- «Специалист по системам защитных покрытий поверхности зданий и сооружений опасных производственных объектов», утвержденного приказом Минтруда России от 13 октября 2014 г. №709н.
На конференции «Качество. Технологии. Инновации» ученые и производственники обсудили проблемы отрасли строительных материалов 27-29 апреля 2021 года в Новосибирском государственном архитектурно-строительном университете (Сибстрин) прошла IV Международная научно-практическая конференция «Качество. |
Хореографический ансамбль «Сибирь» стал победителем одного из самых престижных танцевальных конкурсов и получил титул члена Международного совета по танцу ЮНЕСКО Народному коллективу хореографическому ансамблю «Сибирь» Новосибирского государственного архитектурно-строительного университета (Сибстрин) и его художественному руководителю Наталье Викторовне Бейсеновой присвоен Титул Члена СID UNESCO (Международного совета по танцу ЮНЕСКО). |
В Сибстрине почтили память героев Великой Отечественной войны 11 мая 2021 года на площади перед памятником павшим героям-сибстриновцам состоялась торжественная церемония возложения цветов, посвященная 76-ой годовщине Победы в Великой Отечественной войне.
|
Студенты НГАСУ (Сибстрин) стали победителями соревнований по чир-спорту на Всемирной танцевальной Олимпиаде Представители Новосибирского государственного архитектурно-строительного университета (Сибстрин) заняли первое место во Всероссийских соревнованиях среди студентов по чир-спорту, которые состоялись в рамках XVII Всемирной танцевальной Олимпиады.
|
Методы и способы защиты от коррозии металлов
Проблема изыскания новых и совершенствование старых способов защиты от коррозии актуальна, как для всей тяжёлой промышленности в целом, так и для автомобильной отрасли в частности.
Еще в XIX веке лучшие инженерные умы того времени волновала проблема защиты металлических конструкций от ржавления. Например, Александр Гюста́в Э́йфель, отец и создатель знаменитой «Tour de 300 mètres», говорил: «Трудно переоценить роль краски в сохранении металлического сооружения, и забота об этом – единственная гарантия его долголетия».
Портрет Александра Гюста́ва Э́йфель и его творение — Эйфелева башня
Кстати, вот уже 131 год эта достопримечательность Парижа противостоит воздействию неблагоприятных факторов окружающей среды именно благодаря краске. Интересный факт – для защиты 200.000 м2 наружной поверхности башни используется около 60 тонн специальной краски. Покраской занимается обслуживающая Эйфелеву башню специально созданная компания «SETE» («Société Nouvelle d’exploitation de la Tour Eiffel»). Весь процесс окраски занимает около 18 месяцев! Вначале, все детали конструкции тщательно осматриваются. Те, на которых слой антикоррозионного покрытия нарушен, – очищаются от старого и покрываются новым. Кроме того, вся поверхность сооружения перед окраской очищается паром высокого давления. Красят башню в два слоя.
Интересный факт – для защиты 200.000 м2 наружной поверхности башни используется около 60 тонн специальной краски. Покраской занимается обслуживающая Эйфелеву башню специально созданная компания «SETE» («Société Nouvelle d’exploitation de la Tour Eiffel»). Весь процесс окраски занимает около 18 месяцев! Вначале, все детали конструкции тщательно осматриваются. Те, на которых слой антикоррозионного покрытия нарушен, – очищаются от старого и покрываются новым. Кроме того, вся поверхность сооружения перед окраской очищается паром высокого давления. Красят башню в два слоя.
Но, окрашивание защищаемой поверхности – всего лишь один из способов защиты металла от коррозии. Применительно к автомобилестроению, все методы защиты можно условно разделить на следующие виды:
1. Нанесение защитных покрытий (металлических и неметаллических).
2. Изменение характеристик коррозионной среды.
3. Легирование.
4. Электрохимическая защита
5. Рациональное конструирование.
Нанесение защитных покрытий
Нанесение защитных покрытий – один из самых простых, а также исторических старых способов защиты металла от коррозии. Различают металлические и неметаллические покрытия. В свою очередь неметаллические покрытия делят на органические и неорганические.
Органические покрытия – это, привычные нам, лак и краска, а также разнообразные смолы. Сюда же относят полимерные плёнки и резину.
Неорганические покрытия включают в себя разнообразные эмали и грунты на основе соединений кремния, фосфора, цинка и хрома, а также оксидов металлов (например, оксид титана). Классическим примером использования неорганического покрытия в автомобилестроении является процесс фосфатирования автомобильных кузовов. Так, слоем фосфатов перед покраской покрывают кузова автомобилей на заводах Mercedes-Benz.
Металлические покрытия (анодные и катодные) представляют собой нанесённый на защищаемую поверхность слой металла (цинк, хром, кадмий, алюминий и др. ) или металлического сплава (олово, бронза, латунь и т.д.). У анодного покрытия электродный потенциал меньше электродного потенциала защищаемого металла. Поэтому, при повреждении анодного покрытия в первую очередь будет окисляться непосредственно оно само. В случае с катодным металлическим покрытием – наоборот: электродный потенциал покрытия выше потенциала защищаемого металла. Значит, при повреждении такого покрытия первой будет окисляться сама защищаемая поверхность.
) или металлического сплава (олово, бронза, латунь и т.д.). У анодного покрытия электродный потенциал меньше электродного потенциала защищаемого металла. Поэтому, при повреждении анодного покрытия в первую очередь будет окисляться непосредственно оно само. В случае с катодным металлическим покрытием – наоборот: электродный потенциал покрытия выше потенциала защищаемого металла. Значит, при повреждении такого покрытия первой будет окисляться сама защищаемая поверхность.
Нанесение антикоррозийной защиты Krown
Цинкование
Применительно к автомобилестроению, классическим примером защиты с помощью металлического покрытия является оцинкованный автомобильный кузов. Этот способ получил очень широкое распространение и на сегодняшний день целый ряд автопроизводителей используют цинкование для защиты кузовных деталей. Но, первопроходцем в этом деле стала немецкая компания Audi, впервые применившая оцинковку для защиты кузовов своих автомобилей. Не остановившись на этом, инженеры Audi AG разработали и внедрили в производство двухстороннюю цинковую защиту не только кузовных деталей, но и их сварных соединений, а также и самих кузовов в целом. (Метод т.н. «горячего» цинкования погружением в ванну.) Первым серийным автомобилем с полностью оцинкованным кузовом стал Audi 80 B3, впервые сошедший с конвейера в уже далеком 1986 году.
Не остановившись на этом, инженеры Audi AG разработали и внедрили в производство двухстороннюю цинковую защиту не только кузовных деталей, но и их сварных соединений, а также и самих кузовов в целом. (Метод т.н. «горячего» цинкования погружением в ванну.) Первым серийным автомобилем с полностью оцинкованным кузовом стал Audi 80 B3, впервые сошедший с конвейера в уже далеком 1986 году.
Процесс цинкования
Изменение характеристик коррозионной среды
Изменение характеристик коррозионной среды – суть этого метода защиты заключается в том, что для снижения агрессивности среды в ней уменьшают количество опасных в коррозионном отношении компонентов или же применяют ингибиторы коррозии. (Это специальные вещества, замедляющие её скорость.) И вот, казалось бы, неразрешимая дилемма – как можно снизить количество опасных для стальных деталей автомобиля химических соединений в городской среде? Да очень просто – для начала перестать сыпать на дороги зимой активаторы коррозии, к примеру, тот же хлорид натрия. (О его роли в химическом процессе ржавления автомобиля мы говорили в первой части нашего рассказа.)
(О его роли в химическом процессе ржавления автомобиля мы говорили в первой части нашего рассказа.)
Что касается ингибиторов коррозии, то их целесообразно использовать в замкнутых системах (где редко или мало обновляется циркулирующая жидкость). В автомобилестроении типичным примером таковой является система охлаждения двигателя. А все современные антифризы в обязательном порядке содержат в себе ингибиторы коррозии.
Легирование
Легирование (от немецкого legieren – «сплавлять» и от латинского ligare – «связывать») – один из самых эффективных и, одновременно, дорогих способов борьбы со ржавчиной. Суть этого метода заключается в том, что в состав стали добавляют т.н. «легирующие элементы». Таковыми являются некоторые металлы: хром, никель, марганец, ванадий, ниобий, вольфрам, молибден, титан, медь. Данные компоненты придают сплаву пассивность – т.е. при начале коррозии образуются плотные поверхностные продукты реакции, предохраняющие металл от дальнейшего коррозионного разрушения.
Легированные стали, устойчивые к коррозии в атмосфере и агрессивных средах, также называют «нержавеющими сталями», или же, в простонародье, «нержавейкой». Если говорить об её применении в машиностроении, то нужно сказать, что изготовить кузов автомобиля целиком из нержавеющего сплава, конечно же, возможно. Вот только никакой целесообразности в этом нет, ибо цена такой машины будет астрономической. Причина – изначально высокая стоимость коррозионно-стойкой стали. Тем не менее, в автомобилестроении она активно используется. Так, из неё изготавливают детали системы выпуска отработанных газов и термоотражающие экраны.
Электрохимическая защита
Электрохимическая защита автомобиля
Если говорить о методе электрохимической защиты, то, применительно к автомобилестроению, он является малоиспользуемым. Его суть заключается в торможении протекающих при электрохимической коррозии процессов (катодного / анодного). Например, к защищаемому элементу присоединяется деталь из более активного, нежели сам элемент, металла. В образовавшейся гальванической (коррозионной) паре в первую очередь будет разрушаться активный металл (протектор).
Например, к защищаемому элементу присоединяется деталь из более активного, нежели сам элемент, металла. В образовавшейся гальванической (коррозионной) паре в первую очередь будет разрушаться активный металл (протектор).
А вот метод рационального конструирования, в силу своей относительной простоты и малозатратности, наоборот, получил широкое распространение в машиностроении. Суть его заключается в том, что при проектировании узлов и агрегатов по возможности пытаются уменьшить площадь контакта с агрессивной средой опасных в коррозионном отношении участков деталей (сварных швов и металлических соединений). Если, в силу особенностей конструкции, сделать это не представляется возможным, предусматривают защиту данных узлов от коррозии различными вышеуказанными методами.
Средства защиты коммуникаций от коррозии
Коррозия — это самопроизвольное разрушение металлов в результате химического или физико-химического взаимодействия с окружающей средой. Причиной коррозии служит термодинамическая неустойчивость конструкционных материалов к воздействию веществ, находящихся в контактирующей с ними среде. Скорость коррозии, как и всякой химической реакции, очень сильно зависит от температуры. Повышение температуры на 100 градусов может увеличить скорость коррозии на несколько порядков.
Причиной коррозии служит термодинамическая неустойчивость конструкционных материалов к воздействию веществ, находящихся в контактирующей с ними среде. Скорость коррозии, как и всякой химической реакции, очень сильно зависит от температуры. Повышение температуры на 100 градусов может увеличить скорость коррозии на несколько порядков.
Справка. Антикоррозионная защита
«Мосинжпроект», не являясь профильным институтом, выступил с разработками в области защиты трубопроводов от коррозии и предоставил их в качестве основы для использования при проектировании объектов специалистам МосгазНИИпроекта и МосводоканалНИИпроекта.
Обеспечение антикоррозионной защиты – одно из важных направлений при проектировании, строительстве и эксплуатации объектов городской инженерной инфраструктуры. Актуальными эти вопросы становятся уже на этапе проектирования. Выверенные и обоснованные технические решения, заложенные в проект, гарантируют безопасность и долговременность эксплуатации объекта.
Актуальными эти вопросы становятся уже на этапе проектирования. Выверенные и обоснованные технические решения, заложенные в проект, гарантируют безопасность и долговременность эксплуатации объекта.
Этим направлением инженерии с момента основания «Мосинжпроекта» занимается мастерская №9, в составе которой выделено проектное и одновременно научно-экспериментальное подразделение. Именно «Мосинжпроект», не являясь профильным институтом, выступил с разработками в области защиты трубопроводов от коррозии и предоставил их в качестве основы для использования при проектировании объектов специалистам МосгазНИИпроекта и МосводоканалНИИпроекта.
Специалисты института применяют целый комплекс решений в области антикоррозийной защиты. Выбор конкретного решения зависит от многих факторов, таких как срок предполагаемой службы объекта, район, в котором размещается данный объект, особенности эксплуатации.
Современная защита металлов от коррозии осуществляется с помощью различных методов. Средства защиты можно разделить на две группы:
Средства защиты можно разделить на две группы:
— метод повышения химического сопротивления конструкционных материалов и изоляции поверхности металла от агрессивной среды, который обычно реализуется до начала производственной эксплуатации металлоизделия. Еще на стадии проектирования и изготовления изделия производится выбор конструкционных материалов и их сочетаний, наносятся гальванические и иные защитные покрытия;
— метод понижения агрессивности производственной среды и снижения коррозии наложением внешнего тока. Он осуществляется только в ходе эксплуатации металлоизделия и не связан с какой-либо предварительной обработкой до начала использования. Этот метод подразумевает пропускание тока через металл для достижения защитного потенциала, а также введение в технологическую среду специальных добавок-ингибиторов.
За 55 лет работы «Мосинжпроекта» мастерской выпущено более 4500 тысяч проектов по электрозащите подземных стальных коммуникаций от коррозии. В настоящий момент в Москве работает около 3000 водопроводных УКЗ и более 5000 установок защиты на газопроводных сетях, которые защищают порядка 45000 км стальных газопроводов, водопроводов, канализации и других металлических коммуникаций. За эти годы для Москвы сэкономлены сотни тонн металла.
За эти годы для Москвы сэкономлены сотни тонн металла.
виды, особенности, защита от коррозии
Атмосферная коррозия металлов – один из основных факторов риска при использовании металлоконструкций на открытом воздухе. Процесс начинается под действием внешних факторов и приводит к постепенному разрушению материала.
В этом материале мы расскажем о том, как формируется такой тип коррозии, в чем его опасность и какие средства используют для защиты металла.
Понятие и виды атмосферной коррозии
Появление ржавчины стимулируется микроклиматом, наблюдаемым в нижних слоях атмосферы. Материалы без дополнительной защиты постепенно начинают страдать от такой проблемы.
При этом, атмосферная коррозия не такая стремительная и губительная, как почвенная и морская. Это дает возможность использовать специальные средства для защиты от нее и продлевать длительность эксплуатаций изделий из металла.
Особенность атмосферной коррозии заключается в том, что у разных материалов и в зависимости от климата, ее протекание сильно отличается.
Есть 3 вида атмосферной коррозии:
Сухая атмосферная коррозия
В этом случае повреждение начинается и без воздействия влаги – на поверхности металла не появляется характерной деструктивной пленки из жидкости. Для протекания процесса, нужно чтобы влажность окружающей среды была меньше 60%.
По своей сути процесс – химический. Он слишком стремителен в силу образования окислительного слоя – он постепенно замедляет распространение ржавения внутрь. Аналогичный принцип используется и при пассивации металлов.
Если рассматривать течение процесса подробнее, его делят на два этапа:
- Быстрый. Начинается при соприкосновении необработанного материала с воздухом.
- Медленный. Постепенное протекание ржавения металла после того, как на нем появился слой окислов.

При этом ржавчина, пусть и медленно, но распространяется. Поверхность постепенно темнеет, а структура материала начинает разрушаться, теряет прочность.
Интенсивность протекания процесса будет зависеть от температуры окружающей среды. Если она высокая, скорость увеличится. Толщина пленки варьируется в зависимости от самого материала. Доказано, что дополнительным стимулятором развития процесса становится рассеивание в атмосфере агрессивных газов.
Влажная атмосферная коррозия
Такой тип коррозии стимулируется появлением слоя влаги на металле. Для России такой тип повреждений наиболее характерен. Если влажность воздуха превышает 60%, риск развития коррозийного поражения увеличивается.
Уйти от него невозможно – даже при утреннем выпадении росы влажность уже оказывается достаточной, чтобы покрыть деталь опасной пленкой.
Риск поражения также увеличивается из-за высокого уровня загрязненности воздуха, контакта с агрессивными химическими средами.
Конденсация влаги проходит по трем основным механизмам:
- Химический. Влага начинает накапливаться, потому что коррозийные продукты начинают контактировать с влажным воздухом. Это усугубляет процесс, потому ржавые участки сильнее задерживают воду.
- Капиллярная. Возникает в трещинах, зазорах и щелях.
- Абсорбционная. Связана с действием одноименных сил на стальной поверхности.
Часто в развитии процесса участвуют все три механизма, но на разных этапах его появления. Итог один – материал теряет прочность и постепенно начинает разрушаться.
Мокрая атмосферная коррозия
Быстрый и опасный тип атмосферной коррозии. Начинает появляться при стопроцентной влажности воздуха, когда на металле скапливаются капли воды.
Также процесс характерен и для тех конструкций, которые постоянно помещены в воду. Если вода загрязнена, имеет повышенную кислотность или концентрацию соли, риск только увеличивается.
Как факторы влияют на появление коррозии
Когда мы рассмотрели виды атмосферной коррозии, пришло время внимательнее оценить факторы ее возникновения и развития.
На изделие их может воздействовать сразу несколько, а при усугублении влияния скорость только растет.
Среди распространенных факторов:
Повышенная влажность воздуха
Как уже было описано выше, она создает пленку разной толщины, которая начинает разрушать материал.
Главный параметр – относительная атмосферная влажность. Она начинает значительно влиять на металл, когда уровень превышает 60%.
При стопроцентной влажности, развивается мокрая коррозия, затрагивающая практически все виды материалов.
В зависимости от сплава, критический уровень влажности может меняться. Так сталь, цинк, медь и никель начинают ржаветь при показателях выше 70%.
Техногенное загрязнение воздуха становится дополнительным фактором порчи при влажности.
Газовый состав атмосферы
Можно легко заметить, что при аналогичной влажности, уровне осадков и периодичности туманов, в разных регионах материалы ржавеют с отличной друг от друга скоростью. Причина заключается в составе атмосферы. Рассеянные в ней газы могут значительно ускорять процесс.
Причина заключается в составе атмосферы. Рассеянные в ней газы могут значительно ускорять процесс.
Наиболее опасная среди всех примесей – диоксид серы. Она дает стимулирование скорости процесса в десятки раз. Некоторые виды газов могут выступать как депассиваторы, а также отражаться на поверхности даже если она прошла обработку.
Именно по этой причине, если вы проводите установку металлоконструкции в промышленном районе с большим количеством опасных производств, нужно внимательно выбирать место. Особенно это актуально при использовании нестабильных металлов, таких, как цинк, кадмий или железо.
Также стоит отметить, что при высокой влажности этот негативный фактор только усугубляется.
Уровень содержания твердых частиц
Речь идет как про пассивные, так и про активные включения. Они влияют на электропроводность влаги, стимулируют ее накопление, выступают как депассиваторы.
К наиболее опасным соединениям относятся такие, как (Nh5)2SO4 и Na2SO4. Они могут быть рассеяны в воздухе в виде пыли и легко переносятся ветром. Именно по этой причине рядом с уже сильно проржавевшими металлическими изделиями коррозия начинает развиваться быстрее, чем в обычной обстановке.
Именно по этой причине рядом с уже сильно проржавевшими металлическими изделиями коррозия начинает развиваться быстрее, чем в обычной обстановке.
Температура
Так как в нашей полосе наиболее распространена именно влажная или мокрая коррозия, температура играет важную роль в испарении воды. Когда столбик термометра опускается ниже, происходит медленное испарение воды, а значит, деталь ржавеет быстрее.
Также не стоит забывать и о географическом факторе. Он сочетает в себе все три описанных. В разных регионах отличается влажность, уровень осадков и другие факторы.
Кроме того, меняется состав атмосферы, наличие посторонних крупных включений и загрязнителей. Потому одинаковые по составу сплавы ржавеют с разной скоростью даже в разных районах одного города, не говоря уже о регионе.
Как протекает атмосферная коррозия?
Чтобы перейти к вопросу защиты от атмосферной коррозии, важно рассмотреть сам механизм ее протекания.
Представим металлическую заготовку и попробуем посмотреть на нее через микроскоп.
Так вы быстро увидите сформированную на поверхности тонкую пленку. Это электролит. В зависимости от того, в каких условиях хранился или использовался металл, электролит формируется из продуктов коррозии или атмосферной влаги.
При контакте с воздухом, на материале начинается развитие катодного процесса с параллельным замедлением анодного. Если атмосфера сильно загрязнена, состав электролита может меняться, на него начинают воздействовать агрессивные примеси газов и других частиц.
Когда критическая масса набирается, металл ржавеет. Процесс проникает все глубже внутрь. На финальных стадиях в листах появляются дыры, а металлические детали становятся хрупкими. Большинство механизмов защиты от действия атмосферы направлены на то, чтобы изначально не дать процессу случиться.
Как защититься от атмосферной коррозии
Защита от угрозы повреждения металла – это очень важное условие увеличения длительности эксплуатации изделий. Явление появления ржавчины хорошо изучено и для уменьшения риска используется несколько основных средств:
Явление появления ржавчины хорошо изучено и для уменьшения риска используется несколько основных средств:
- Нанесение специальных покрытий. Они могут быть как металлическими, так и неметаллическими. При нанесении металлического используется цинк, никель и другие материалы. К неметаллической группе относятся многочисленные смазки, ЛКП, специальные пасты. Многие из них могут применяться не только для защиты, но и в качестве ингибиторов атмосферной коррозии на уже пораженных деталях. Так удается замедлить или блокировать распространение разрушения.
- Стабилизация уровня влажности воздуха. При условии, что воздух чистый, без сильной концентрации вредных примесей, опасных паров, уровень относительной влажности можно поддерживать на отметке в 50%. Это не устранит опасности развития сухой коррозии, но общий риск порчи значительно уменьшит.
- Использование ингибиторов. Так называются вещества, которые способны замедлить или заблокировать распространение коррозийного поражения.
 Обычно используются вещества летучего типа – от нитритов и бензоатов до карбонатов. Они могут применяться в различных видах – от пропитки до закачивания внутрь металлической емкости.
Обычно используются вещества летучего типа – от нитритов и бензоатов до карбонатов. Они могут применяться в различных видах – от пропитки до закачивания внутрь металлической емкости. - Легирование. Обеспечивается на этапе выплавки стали. Такие вещества как медь, хром, никель, титан и некоторые другие помогают существенно уменьшить скорость анодной реакции. На выходе металлу также будет требоваться дополнительная защита, но и сам по себе он хорошо противостоит угрозе.
Мы знаем, как защитить материал от порчи
Так как распространение ржавчины нужно не допустить – она может полностью вывести из строя металлическое изделие, намного выгоднее изначально подумать о правильной защите. Мы справляемся с задачей методом цинкования. Он помогает создать на поверхности защитный слой, который не допускает контакта с воздухом и водой.
У нас три цеха горячего цинкования и самая глубокая ванна в Центральном федеральном округе. Это позволяет выполнять крупные заказы и работать с массивными изделиями.
Оставьте заявку на сайте или звоните нам, чтобы оформить заказ услуги или получить ответы на интересующие вас вопросы.
Вернуться к статьям
Поделиться статьей
Основы коррозии — NACE
Коррозия — естественный, но контролируемый процесс
Гретхен А. Якобсон — Работа с материалами Ответственный редактор
Коррозия — это естественное явление, обычно определяемое как разрушение материала (обычно металла) в результате химической или электрохимической реакции с окружающей средой. 1 Подобно другим стихийным бедствиям, таким как землетрясения или суровые погодные условия, коррозия может нанести опасный и дорогостоящий ущерб всему: от автомобилей, бытовой техники, систем водоснабжения и канализации до трубопроводов, мостов и общественных зданий. Однако, в отличие от стихийных бедствий, связанных с погодой, существуют проверенные временем методы предотвращения и контроля коррозии, которые могут уменьшить или устранить ее воздействие на общественную безопасность, экономику и окружающую среду.
Однако, в отличие от стихийных бедствий, связанных с погодой, существуют проверенные временем методы предотвращения и контроля коррозии, которые могут уменьшить или устранить ее воздействие на общественную безопасность, экономику и окружающую среду.
Наука о предотвращении и контроле коррозии очень сложна и усугубляется тем фактом, что коррозия принимает множество различных форм и зависит от множества внешних факторов. Специалисты по коррозии должны понимать влияние условий окружающей среды, таких как удельное сопротивление почвы, влажность и воздействие соленой воды на различные типы материалов; тип продукта, который будет обрабатываться, обрабатываться или транспортироваться; требуемый срок службы конструкции или компонента; близость к явлениям, вызывающим коррозию, таким как паразитный ток от железнодорожных систем; соответствующие методы смягчения последствий; и другие соображения, прежде чем определять конкретную проблему коррозии и определять эффективное решение.
Однако первым шагом к эффективному контролю за коррозией является получение доскональных знаний о различных формах коррозии, задействованных механизмах, способах их обнаружения, а также о том, как и почему они возникают. 2
2
Проще говоря, коррозия — это естественное разрушение, которое возникает, когда поверхность вступает в реакцию с окружающей средой. Различные поверхности, окружающая среда и другие факторы добавляют сложности к уравнению.
Список литературы
1. Основы коррозии, Введение, L.С. Ван Делиндер, изд. (Хьюстон, Техас: NACE, 1984).
2. Пособие по международному базовому курсу NACE по коррозии (Хьюстон, Техас: NACE, 2000).
Факторы
Профилактика и контроль требуют рассмотрения многих факторов, прежде чем определять конкретную проблему и эффективное решение, включая, но не ограничиваясь:
- Условия окружающей среды, такие как удельное сопротивление почвы, влажность и воздействие соленой воды на различные типы материалов
- вид продукции, подлежащей переработке, погрузке-разгрузке или транспортировке
- Требуемый срок службы конструкции или компонента
- близость к явлениям, вызывающим коррозию, таким как паразитный ток от рельсовых систем
- соответствующие методы смягчения последствий
Коррозия общей атаки
Также называемая «общая коррозия» или «равномерная коррозия», общая коррозионная коррозия протекает более или менее равномерно по открытой поверхности без заметной локализации.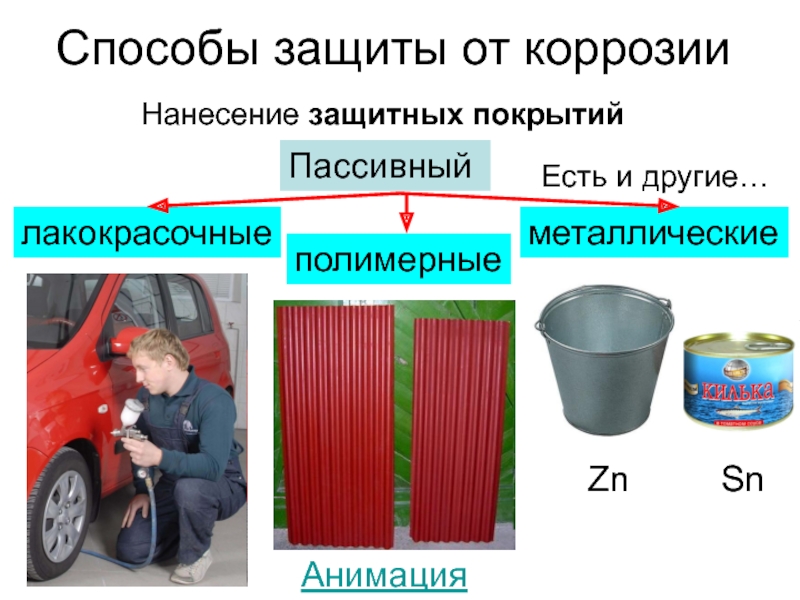 Это приводит к относительно равномерному утонению листовых и листовых материалов и общему утонению с одной или другой стороны (или обеих) труб и насосно-компрессорных труб. Это определяется по шероховатости поверхности и, как правило, по наличию продуктов коррозии. Механизм атаки обычно представляет собой электрохимический процесс, происходящий на поверхности материала. Различия в составе или ориентации небольших участков на поверхности металла создают аноды и катоды, которые облегчают процесс коррозии.
Это приводит к относительно равномерному утонению листовых и листовых материалов и общему утонению с одной или другой стороны (или обеих) труб и насосно-компрессорных труб. Это определяется по шероховатости поверхности и, как правило, по наличию продуктов коррозии. Механизм атаки обычно представляет собой электрохимический процесс, происходящий на поверхности материала. Различия в составе или ориентации небольших участков на поверхности металла создают аноды и катоды, которые облегчают процесс коррозии.
Чаще всего вызванная неправильным применением материалов в коррозионных средах, общая коррозия часто допустима, потому что эффект потери металла относительно легко оценить, и при первоначальном проектировании можно сделать поправки. Защитные покрытия особенно эффективны в борьбе с равномерной коррозией. Катодная защита (CP) — электрохимический метод, используемый для контроля коррозии (см. «Методы контроля коррозии» далее в этой статье), — может использоваться в подземных условиях или в условиях погружения.
Локальная коррозия
В отличие от общей агрессивной коррозии, локальная коррозия возникает на отдельных участках металлической поверхности. Типы локальной коррозии включают точечную, щелевую и нитевидную коррозию.
Десять базовых форм
Существует 10 основных форм коррозии, но редко когда корродирующая конструкция или компонент страдает только от одной. Комбинация металлов, используемых в системе, и широкий спектр встречающихся сред часто вызывают более одного типа атак.Даже один сплав может подвергаться коррозии в нескольких формах в зависимости от его воздействия в различных средах в разных точках системы.
Все формы коррозии, за исключением некоторых видов высокотемпературной коррозии, возникают под действием электрохимической ячейки (рис. 1). Общие для всех ячеек коррозии элементы — это анод, на котором происходит окисление и потеря металла, катод, на котором возникают восстановительные и защитные эффекты, металлические и электролитические пути между анодом и катодом, через которые протекает электронный и ионный ток, и разность потенциалов, которая двигает ячейку. Движущий потенциал может быть результатом различий между характеристиками разнородных металлов, условиями поверхности и окружающей средой, включая химические концентрации. Существуют определенные механизмы, вызывающие каждый тип атак, различные способы их измерения и прогнозирования, а также различные методы, которые можно использовать для контроля коррозии в каждой из ее форм.
Движущий потенциал может быть результатом различий между характеристиками разнородных металлов, условиями поверхности и окружающей средой, включая химические концентрации. Существуют определенные механизмы, вызывающие каждый тип атак, различные способы их измерения и прогнозирования, а также различные методы, которые можно использовать для контроля коррозии в каждой из ее форм.
Рисунок 1: Электрохимическая ячейка В коррозионной ячейке электроны проходят по металлическому пути от участков, где происходят анодные реакции, к участкам, где они позволяют протекать катодным реакциям.Ионы (заряженные частицы) проходят через электролит, чтобы уравновесить поток электронов. Анионы (отрицательно заряженные ионы от катодных реакций) текут к аноду, а катионы (положительно заряженные ионы от самого анода) текут к катоду. Анод подвергается коррозии, а катод — нет. Также существует разница напряжения или потенциала между анодом и катодом. Источник: Справочник международного базового курса по коррозии NACE, стр. 2: 9.
2: 9.
Коррозия и защита от коррозии — Служба транспортной информации
Явление коррозии
Коррозия — это термин, используемый для описания ухудшения качества обычно металлического материала из-за химического или электрохимического воздействия.Коррозия теперь также используется для описания аналогичного воздействия на другие материалы, такие как стекло, пластик, строительные материалы. Агрессивная среда известна как коррозионный агент. DIN 50900 выделяет следующие типы коррозии:
| Равномерная поверхностная коррозия, при которой поверхность имеет равномерные повреждения. | |
| Широкая ямка, при которой поверхность имеет повреждения разной степени тяжести. | |
| Точечная коррозия, при которой разрушаются только небольшие участки поверхности. | |
Гальваническая коррозия, при которой небольшие участки поверхности подвергаются воздействию трещин. |
Рисунок 1 | Рисунок 2 |
Вернуться к началу
Причина коррозии
Вернуться к началу
Предварительная обработка и очистка предметов для упаковки
Существует мало информации о том, насколько тщательно следует очищать металлические компоненты перед нанесением защиты от коррозии методы.Тщательная предварительная обработка и очистка необходимы, если методы защиты от коррозии в любом случае будут успешными. Если все частицы грязи и пыли, а также остатки кислоты и соли не будут полностью удалены, а предмет полностью высохнет, например, при использовании метода защитного покрытия, под защитным покрытием может возникнуть коррозия.
Очистка выполняется либо водой, которая, в зависимости от очищаемого предмета, может содержать определенные добавки, либо растворителями, которые, будучи универсальными очистителями, могут использоваться в большем количестве применений. После очистки водой или растворителями очищенные предметы сушатся перед дальнейшей обработкой. На этом этапе необходимо следить за тем, чтобы не допустить дальнейшего загрязнения, например, следы пальцев, происходит.
После очистки водой или растворителями очищенные предметы сушатся перед дальнейшей обработкой. На этом этапе необходимо следить за тем, чтобы не допустить дальнейшего загрязнения, например, следы пальцев, происходит.
Вернуться к началу
Коррозия и окружающая среда
Коррозия и окружающая среда
Коррозия — это разрушающее воздействие на материалреакция с окружающей средой.Серьезные последствия коррозии процесса стали проблемой мирового значения. В дополнение к наши повседневные встречи с этой формой деградации, причины коррозии остановки завода, растрата ценных ресурсов, потеря или загрязнение продукт, снижение эффективности, дорогостоящее обслуживание и дорогостоящая переделка. Это также может поставить под угрозу безопасность и препятствовать техническому прогрессу. |
Шаг 1 железо + кислород -> оксид железа
Шаг 2 оксид железа + вода -> гидратированный оксид железа (ржавчина)
Коррозия атмосферная окисление металлов. образует новый слой. Этот слой может быть хорошим или плохим. Безусловно, самый важный Форма коррозии — ржавление железа и стали. Ржавчина — это процесс окисления, при котором железо соединяется с водой и кислородом с образованием ржавчины, красновато-коричневая корка, образующаяся на поверхности железа. Так как железо настолько широко используется, например, в строительстве и в производстве инструментов, что его защита от ржавления важна.Ржавчину можно предотвратить, исключив воздух и вода с поверхности железа, например, путем окраски, смазки или смазки, или покрывая утюг защитным покрытием из другого металла. Многие сплавы железа устойчивы к коррозии. Нержавеющие стали — это сплавы железа с такими металлами, как хром и никель; они не разъедают, потому что добавленные металлы помогают формировать твердое, прочное оксидное покрытие, устойчивое к дальнейшая атака. |
Хотя такие металлы, как алюминий, хром и цинк, корродируютих оксиды легче, чем железо, образуют покрытие, защищающее металл от дальнейшего нападения. Ржавчина хрупкая и отслаивается от поверхности. утюга, постоянно обнажая свежую поверхность. Таким образом, эти металлы могут быть лучшим выбором для продукта, который будет подвержен ржавчине условия, такие как вода и воздух. |
Распознавание симптомов и механизма коррозиипроблема — важный предварительный шаг на пути к поиску удобного решение. Существует пять основных методов борьбы с коррозией:
|
Влияние покрытия на коррозию и катодную защиту
Четыре основных элемента коррозионной ячейки — это анод, катод, а также металлические и электролитические пути между ними. Борьба с коррозией может быть достигнута путем устранения (или уменьшения) любого из этих элементов.
Борьба с коррозией может быть достигнута путем устранения (или уменьшения) любого из этих элементов.
Одним из таких методов является изменение пути электролита путем создания барьера между металлической поверхностью, находящейся под угрозой, и коррозионной средой (т.е. путем нанесения какого-либо покрытия). Если бы все металлические поверхности могли быть покрыты материалом, который был бы абсолютно водонепроницаемым и абсолютно без изъянов (пропусков), все атаки были бы остановлены. Следует отметить, что эти два свойства должны быть постоянными без ухудшения качества.
К сожалению, никакая комбинация материалов покрытия и кропотливого нанесения не может гарантировать безупречное покрытие на неопределенный срок. Однако есть современные покрытия, которые приближаются к совершенству, но по все более высокой цене. Часто практичнее всего признать неизбежность некоторых дефектов покрытия, когда коррозию можно контролировать с помощью катодной защиты (CP).
Затраты, связанные с CP для различных диапазонов эффективности покрытия, хорошо известны. Таким образом, можно выбрать рентабельную комбинацию достаточно хорошего покрытия и CP, имея в виду, что, как правило, нецелесообразно увеличивать инвестиции в более качественное покрытие сверх соответствующей экономии затрат на CP.Поэтому возникает несколько вопросов об использовании несовершенных покрытий:
Таким образом, можно выбрать рентабельную комбинацию достаточно хорошего покрытия и CP, имея в виду, что, как правило, нецелесообразно увеличивать инвестиции в более качественное покрытие сверх соответствующей экономии затрат на CP.Поэтому возникает несколько вопросов об использовании несовершенных покрытий:
• Насколько хороши они, когда используются по отдельности?
• Как они влияют на развитие коррозии?
• Как они влияют на потребность в CP?
Трубопроводы нерегулируемые без КП
По сравнению с неизолированным трубопроводом в той же среде можно ожидать, что линия с покрытием будет иметь меньше утечек в течение срока службы; однако в линии с покрытием может произойти первая утечка раньше, потому что коррозионная активность может быть сконцентрирована на ограниченной площади поверхности при небольших выходах.
При особых обстоятельствах этот эффект может быть еще более выраженным. Предположим, что после нескольких лет эксплуатации в неизолированной линии возникает утечка в наиболее агрессивном месте, требующем ремонта или замены. Коррозионная среда будет усугубляться тенденцией новой стали быть более активной (анодной) по сравнению с более старой сталью, а неблагоприятное соотношение площадей анодной и катодной поверхностей приводит к концентрации тока коррозии и большей скорости коррозии.
Решение избежать этой предсказуемой ситуации за счет покрытия нового трубопровода на самом деле только усугубляет ситуацию! Поскольку покрытие не является идеальным, часть новой стали будет контактировать с электролитом, а оставшийся ток коррозии в дальнейшем будет концентрироваться на небольшой площади поверхности, где могут произойти отказы за короткое время.
Установки
Limited CP, использующие протекторные аноды, часто называемые защитой от «горячих точек», могут обеспечить недорогое решение в этой ситуации. В областях, подверженных воздействию паразитного тока, чрезвычайно важно нанести хорошее покрытие на линию в области приема тока (которое является катодным и не подвержено атакам), чтобы увеличить электрическое сопротивление и, таким образом, минимизировать количество потребляемого тока. металл трубы, когда он разряжается в другом месте. В случаях статических блуждающих токов (например,g., катодные паразитные токи), идентификация областей наводки относительно проста.
Однако, когда задействованы динамические паразитные токи (например, около транспортных систем, работающих на постоянном токе), места рядом с путями, которые накапливают паразитный ток, когда поезд находится поблизости, могут фактически разряжать ток обратно на рельсы, когда в этом районе нет нагрузки. Непроизвольное покрытие этих участков без полного понимания характера активности блуждающего тока может сконцентрировать уменьшенный общий ток до недопустимых плотностей.
с CP
Влияние покрытия на требования к CP простое, и его можно кратко сформулировать: нанесение покрытия значительно снижает количество тока, необходимого для получения защиты. Уменьшение может составлять от 99,8% для очень хорошего покрытия до 50% для очень плохого, старого, поврежденного покрытия. Кроме того, хорошее покрытие может значительно улучшить характеристики затухания в трубопроводе, значительно увеличивая эффективный диапазон для отдельного источника защитного тока.
Эта статья адаптирована из книги Corrosion Basics — An Introduction , Second Edition , Pierre R. Roberge, ed. (Хьюстон, Техас: NACE International, 2006), стр. 178-179.
5 способов предотвращения коррозии металлических деталей
Ни один металл не является полностью защищенным от угрозы коррозии. Но можно замедлить, контролировать или остановить коррозию до того, как она вызовет проблему.
Существуют практические способы предотвращения коррозии металлических деталей.Инженеры могут включить контроль коррозии в процесс проектирования. Производители могут применять защитные барьеры от коррозии. Наконец, люди, использующие деталь, могут предпринять профилактические меры, чтобы продлить срок ее службы.
Запросить ценовое предложение
Что такое коррозия?
Коррозия возникает, когда металл вступает в реакцию с окислителем в окружающей его среде. Эта химическая реакция может привести к разрушению металла со временем, потускнению его внешнего вида и нарушению его структурной целостности.
Каждый тип металла имеет разные электрохимические свойства. Эти свойства определяют типы коррозии, которой подвержена деталь. Например, железные инструменты подвержены ржавчине от длительного воздействия влаги, а медная крыша потускнеет под воздействием погоды. Хотя некоторые металлы лучше сопротивляются коррозии, чем другие (в зависимости от окружающей среды), ни один из них не свободен от всех типов коррозии.
Не существует универсального решения для предотвращения коррозии металлических деталей.С таким количеством типов металлов и тысячами возможных применений производители должны использовать различные методы для предотвращения и контроля коррозии в различных металлах.
Способы предотвращения коррозии металлических деталей
Предотвращение коррозии металлических деталей учитывается на всех этапах технологического процесса, от проектирования и изготовления до отделки и обслуживания.
Запросить ценовое предложение
1.Типовой проект дома
Контроль коррозии начинается еще на стадии проектирования. Если деталь предназначена для использования в среде, подверженной коррозии, производители должны проектировать деталь с учетом этого.
Например, части, подверженные воздействию элементов, должны позволять воде и мусору стекать, а не собираться на поверхности. Чтобы уменьшить щелевую коррозию, проектировщики должны устранить узкие зазоры, которые позволяют воздуху или жидкости проникать и застаиваться. Для агрессивных сред, например, в соленой воде, может быть разумно спроектировать некоторый допуск на коррозию.
2. Защитное покрытие
Покрытия
могут обеспечить слой защиты от коррозии, действуя как физический барьер между металлическими частями и окисляющими элементами в окружающей среде. Один из распространенных методов — гальванизация, при которой производители покрывают деталь тонким слоем цинка.
Порошковые покрытия — еще один эффективный способ предотвращения коррозии металлических деталей. При правильном применении порошковое покрытие может изолировать поверхность детали от окружающей среды для защиты от коррозии.
3. Экологический контроль
Многие факторы окружающей среды влияют на вероятность коррозии. Это помогает хранить металлические части в чистом и сухом месте, когда они не используются. Если вы собираетесь хранить их в течение длительного времени, подумайте об использовании методов контроля уровня серы, хлорида или кислорода в окружающей среде.
Гальваническая коррозия возникает, когда металлические детали с двумя разными потенциалами электродов находятся в контакте с электролитом, таким как соленая вода.Это вызывает коррозию металла с более высокой активностью электрода в точке контакта. Можно предотвратить гальваническую коррозию, если хранить эти детали отдельно. Этот эффект также может работать как средство защиты от коррозии, как описано ниже.
Запросить ценовое предложение
4. Катодная защита
Можно предотвратить коррозию, подавая на поверхность металла противоположный электрический ток. Один из методов катодной защиты — это приложенный ток с использованием внешнего протекания электрического тока для подавления коррозионного тока в детали.
Менее сложным методом катодной защиты от коррозии является использование расходуемого анода. Это включает в себя прикрепление небольшого реактивного металла к детали, которую вы хотите защитить. Ионы металла будут течь от химически активного металла к менее активной части, уменьшая коррозию за счет меньшей части.
5. Техническое обслуживание
Защитные покрытия, контроль окружающей среды и катодная защита — эффективные способы предотвращения коррозии металлических деталей.Однако эти меры ничто без постоянного обслуживания и мониторинга. Покрытия могут со временем изнашиваться; даже небольшие зазубрины и царапины могут привести к коррозии. Обязательно содержите детали в чистоте и при необходимости применяйте дополнительную защиту.
1 Коррозия — ее влияние и контроль | Возможности исследований в области науки и техники коррозии
Ядерные реакторные системы
Коммерческие и военные ядерные реакторы испытали широкий спектр проблем с коррозией за последние 55 лет, и, начиная с 1960-х годов, исследования коррозии нашли хорошее применение для смягчения и решения этих проблем.Все действующие предприятия в Соединенных Штатах используют обычную легкую воду с небольшим количеством примесей, но, тем не менее, они на удивление подвержены коррозии.
В системах реакторов с кипящей водой преобладающей проблемой было межкристаллитное коррозионное растрескивание под напряжением (SCC) в аустенитной нержавеющей стали 304, сенсибилизированной сваркой, что приводило к серьезным простоям оборудования. Эта ситуация была изменена осознанием того, что растрескивание можно контролировать, изменяя химический состав воды и состояние увлажненных поверхностей установки.
Во-первых, было снижено содержание примесей в воде; затем вводили водород в нежелательно высоких концентрациях, чтобы снизить коррозионный потенциал стали. Затем, в классическом применении науки о коррозии, было показано, что влажное осаждение благородных металлов на поверхности растений может обеспечить аналогичный уровень защиты с гораздо более низким содержанием водорода. Все эти практические меры по смягчению последствий были поддержаны обширными научными исследованиями в области коррозии, включая разработку датчиков на месте для мониторинга содержания водорода, электродного потенциала и скорости роста трещин.
В реакторах с водой под давлением проблемы коррозии были связаны в основном с парогенераторами, где сплав 600 на основе никеля первоначально использовался для труб, отделяющих воду теплоносителя первого контура от воды, которая кипятится для привода турбин. Это оказалось плохим выбором, потому что материал был подвержен SCC с обеих сторон. Однако меры по исправлению положения — включая термическую обработку материала труб, замену трубок новым сплавом и уменьшение отложений шлама, возникающего из-за примесей в питательной воде, — продлили срок службы парогенераторов.
В процессе этого смягчения последствий были проведены превосходные исследования в поддержку критических вопросов в области металлургии, химического машиностроения, науки о коррозии и даже геохимии. Теперь отрасль находится в таком положении, что она может — с достаточной уверенностью — прогнозировать чрезвычайно долгий срок службы своих новых станций, а также превышать целевые показатели по продлению срока службы отремонтированных станций.
Оба типа ядерных установок столкнулись с проблемами SCC облученного нейтронами материала в активной зоне, и некоторые из самых амбициозных исследований коррозии за последние два десятилетия имели дело с полученным сочетанием изменения свойств материала, микроструктуры и поведения SCC с использованием достижений в моделировании и характеристике.В результате экспериментов и фундаментальных исследований срок службы материала можно предсказать более точно, и существуют рекомендации для новых сплавов с повышенной устойчивостью к этой специализированной форме SCC. Конечная цель — количественное прогнозирование срока службы после полного понимания механизмов коррозии и деградации.
17.6 Коррозия — химия
Цели обучения
К концу этого раздела вы сможете:
- Определить коррозию
- Перечислите некоторые методы, используемые для предотвращения или замедления коррозии.
Коррозия обычно определяется как разложение металлов в результате электрохимического процесса.Образование ржавчины на железе, потускнение серебра и сине-зеленая патина на меди — все это примеры коррозии. Общие затраты на коррозию в Соединенных Штатах значительны и оцениваются более чем в полтриллиона долларов в год.
Статуя Свободы: меняя цвета
Статуя Свободы — достопримечательность, которую признает каждый американец. Статую Свободы легко узнать по ее высоте, положению и уникальному сине-зеленому цвету (рис. 1). Когда эта статуя впервые была доставлена из Франции, она не имела зеленого цвета.Оно было коричневым, цвета его медной «кожи». Так как же Статуя Свободы изменила цвет? Изменение внешнего вида было прямым результатом коррозии. Медь, которая является основным компонентом статуи, медленно подвергалась окислению на воздухе. Окислительно-восстановительные реакции металлической меди в окружающей среде протекают в несколько стадий. Металлическая медь окисляется до оксида меди (I) (Cu 2 O), который имеет красный цвет, а затем до оксида меди (II), который имеет черный цвет
.
[латекс] \ begin {array} {r @ {{} \ longrightarrow {}} ll} 2 \ text {Cu} (s) \; + \; \ frac {1} {2} \ text {O} _2 (g) & \ text {Cu} _2 \ text {O} (s) & (\ text {red}) \\ [0.5em] \ text {Cu} _2 \ text {O} (s) \; + \; \ frac {1} {2} \ text {O} _2 (g) & 2 \ text {CuO} (s) & ( \ text {черный}) \ end {array} [/ latex]
Уголь, часто содержащий большое количество серы, активно сжигался в начале прошлого века. В результате триоксид серы, диоксид углерода и вода реагировали с CuO
.
[латекс] \ begin {array} {r @ {{} = {}} ll} 2 \ text {CuO} (s) \; + \; \ text {CO} _2 (g) \; + \; \ текст {H} _2 \ text {O} (l) & \ text {Cu} _2 \ text {CO} _3 (\ text {OH}) _ 2 (s) & (\ text {зеленый}) \\ [0.5em ] 3 \ text {CuO} (s) \; + \; 2 \ text {CO} _2 (g) \; + \; \ text {H} _2 \ text {O} (l) & \ text {Cu} _2 (\ text {CO} _3) _2 (\ text {OH}) _ 2 (s) & (\ text {blue}) \\ [0.5em] 4 \ text {CuO} (s) \; + \; \ text {SO} _3 (g) \; + \; 3 \ text {H} _2 \ text {O} (l) & \ text {Cu } _4 \ text {SO} _4 (\ text {OH}) _ 6 (s) & (\ text {green}) \ end {array} [/ latex]
Эти три соединения ответственны за характерную сине-зеленую патину, наблюдаемую сегодня. К счастью, патина создала защитный слой на поверхности, предотвращающий дальнейшую коррозию медной пленки. Формирование защитного слоя — это форма пассивации, которая обсуждается далее в следующей главе.
Рисунок 1. (a) Статуя Свободы покрыта медной кожей и изначально была коричневой, как показано на этой картине. {\ circ} = -0.{+} (водн.) [/ латекс]
Количество молекул воды варьируется, поэтому оно представлено как x . В отличие от патины на меди, образование ржавчины не создает защитного слоя, поэтому коррозия железа продолжается, поскольку ржавчина отслаивается и подвергает свежее железо воздействию атмосферы.
Рис. 2. Когда краска поцарапана на окрашенной железной поверхности, возникает коррозия и начинает образовываться ржавчина. Скорость самопроизвольной реакции увеличивается в присутствии электролитов, таких как хлорид натрия, используемый на дорогах для таяния льда и снега или в соленой воде.
Один из способов предохранить железо от коррозии — это держать его в краске. Слой краски предотвращает попадание воды и кислорода, необходимых для образования ржавчины, на утюг. Пока краска остается неповрежденной, утюг защищен от коррозии.
Другие стратегии включают сплавление железа с другими металлами. Например, нержавеющая сталь — это в основном железо с небольшим содержанием хрома. Хром имеет тенденцию собираться у поверхности, где он образует оксидный слой, защищающий железо.
Оцинкованное железо или оцинкованное железо использует другую стратегию. Цинк окисляется легче, чем железо, потому что цинк имеет более низкий восстановительный потенциал. Поскольку цинк имеет более низкий восстановительный потенциал, это более активный металл. Таким образом, даже если цинковое покрытие поцарапано, цинк все равно будет окисляться раньше железа. Это говорит о том, что этот подход должен работать с другими активными металлами.
Еще один важный способ защиты металла — это сделать его катодом в гальваническом элементе.Это катодная защита , которая может использоваться не только для железа, но и для других металлов. Например, ржавление подземных резервуаров для хранения железа и труб можно предотвратить или значительно уменьшить, подключив их к более активному металлу, такому как цинк или магний (рис. 3). Это также используется для защиты металлических частей водонагревателей. Более активные металлы (более низкий потенциал восстановления) называются расходуемыми анодами , потому что по мере их использования они корродируют (окисляются) на аноде.Защищаемый металл служит катодом и поэтому не окисляется (не корродирует). Когда аноды подвергаются надлежащему контролю и периодически заменяются, полезный срок службы резервуара для хранения железа может быть значительно увеличен.
Рис. 3. Одним из способов защиты подземного резервуара для хранения железа является катодная защита. Использование в качестве анода активного металла, такого как цинк или магний, эффективно превращает резервуар для хранения в катод, предотвращая его коррозию (окисление).
Коррозия — это разрушение металла, вызванное электрохимическим процессом.Ежегодно тратятся большие суммы денег на устранение последствий или предотвращение коррозии. Некоторые металлы, такие как алюминий и медь, образуют защитный слой при коррозии на воздухе. Тонкий слой, который образуется на поверхности металла, предотвращает контакт кислорода с большим количеством атомов металла и, таким образом, «защищает» оставшийся металл от дальнейшей коррозии. Железо разъедает (образует ржавчину) под воздействием воды и кислорода. Ржавчина, образующаяся на металлическом железе, отслаивается, обнажая свежий металл, который также подвергается коррозии.Один из способов предотвратить или замедлить коррозию — нанести на металл покрытие. Покрытие предотвращает контакт воды и кислорода с металлом. Краска или другие покрытия замедляют коррозию, но они неэффективны после царапин. Оцинкованное или оцинкованное железо использует тот факт, что цинк более склонен к окислению, чем железо. Пока покрытие остается, даже если оно поцарапано, цинк будет окисляться раньше железа. Еще один метод защиты металлов — катодная защита. В этом методе легко окисляемый и недорогой металл, часто цинк или магний (расходуемый анод), электрически соединяется с металлом, который необходимо защищать.Более активный металл — это расходуемый анод, который является анодом в гальванической ячейке. «Защищенный» металл — это катод, и он остается неокисленным. Одним из преимуществ катодной защиты является то, что расходуемый анод можно контролировать и при необходимости заменять.
Химия: упражнения в конце главы
- Какой элемент каждой пары металлов более склонен к коррозии (окислению)?
(а) Mg или Ca
(б) Au или Hg
(c) Fe или Zn
(d) Ag или Pt
- Рассмотрим следующие металлы: Ag, Au, Mg, Ni и Zn.{\ circ} = -0,477 \; \ text {V}) [/ latex], и все же, когда оба подвергаются воздействию окружающей среды, необработанный алюминий имеет очень хорошую коррозионную стойкость, в то время как коррозионная стойкость необработанного железа плохая. Объясните это наблюдение.
- Если образец железа и образец цинка соприкасаются, цинк разъедает, а железо — нет. Если образец железа соприкасается с образцом меди, железо разъедает, а медь — нет. Объясните этот феномен.
- Предположим, у вас есть три разных металла: A, B и C.{\ circ} = -3.04 \; \ text {V} [/ latex], который, кажется, может защитить все другие металлы, перечисленные в стандартной таблице восстановительного потенциала?
Глоссарий
- катодная защита
- способ защиты металла с помощью расходуемого анода и эффективного получения металла, который требует защиты катода, таким образом предотвращая его окисление
- коррозия
- Разложение металла в результате электрохимического процесса
- оцинкованное железо
- способ защиты железа путем покрытия его цинком, который окисляется раньше железа; оцинкованное железо
- расходуемый анод
- более активный и недорогой металл, используемый в качестве анода в катодной защите; часто из магния или цинка
Решения
Ответы на упражнения в конце главы по химии
2.Mg и Zn
4. Оба примера включают катодную защиту. (Жертвенный) анод — это металл, который коррозирует (окисляется или вступает в реакцию). В случае железа (-0,447 В) и цинка (-0,7618 В) цинк имеет более отрицательный стандартный восстановительный потенциал и поэтому служит анодом. В случае железа и меди (0,34 В) железо имеет меньший стандартный восстановительный потенциал и поэтому подвергается коррозии (служит анодом).
6. Хотя восстановительный потенциал лития делает его способным защищать другие металлы, этот высокий потенциал также указывает на то, насколько литий реакционноспособен; он будет иметь спонтанную реакцию с большинством веществ.Это означает, что литий будет быстро реагировать с другими веществами, даже с теми, которые не окисляют металл, который он пытается защитить. Такая реактивность означает, что расходуемый анод будет быстро истощаться и его нужно будет часто заменять. (Необязательная дополнительная причина: опасность возгорания в присутствии воды.)
.


 Технологии. Инновации», организатором которой выступила кафедра Строительных материалов, стандартизации и сертификации при поддержке лакокрасочного завода «Колорит» (г. Новосибирск).
Технологии. Инновации», организатором которой выступила кафедра Строительных материалов, стандартизации и сертификации при поддержке лакокрасочного завода «Колорит» (г. Новосибирск).
 Также коллектив вуза стал Лауреатом 1 степени одного из самых престижных танцевальных конкурсов в стране – Международного конкурса хореографических искусств «Танцемания 2021».
Также коллектив вуза стал Лауреатом 1 степени одного из самых престижных танцевальных конкурсов в стране – Международного конкурса хореографических искусств «Танцемания 2021».
 В это же время самоотверженным трудом в тылу ученые Сибстрина внесли весомый вклад в развитие строительной науки, так необходимой для укрепления обороноспособности страны. Традиция чтить и передавать из поколение в поколение память о них – была, есть и будет в НГАСУ (Сибстрин)…
В это же время самоотверженным трудом в тылу ученые Сибстрина внесли весомый вклад в развитие строительной науки, так необходимой для укрепления обороноспособности страны. Традиция чтить и передавать из поколение в поколение память о них – была, есть и будет в НГАСУ (Сибстрин)… В число 60 дисциплин соревнований входит чир-спорт – официально признанный вид спорта, который включает в себя различные хореографические и акробатические элементы…
В число 60 дисциплин соревнований входит чир-спорт – официально признанный вид спорта, который включает в себя различные хореографические и акробатические элементы…

 Обычно используются вещества летучего типа – от нитритов и бензоатов до карбонатов. Они могут применяться в различных видах – от пропитки до закачивания внутрь металлической емкости.
Обычно используются вещества летучего типа – от нитритов и бензоатов до карбонатов. Они могут применяться в различных видах – от пропитки до закачивания внутрь металлической емкости. Это означает, что кислород соединяется с металлом и
Это означает, что кислород соединяется с металлом и
